- ユニケミートップ
- Uni-Lab(分析技術情報)
- 周期表とは – 曲がってて、よかった - おまけの章
周期表とは – 曲がってて、よかった - おまけの章

通気性があるのに、水が漏れないオムツとか通気性があるのに、防水性がある生地とか、相反する性質を併せ持つ、ちょっと不思議な素材を見聞きしたことありませんか?
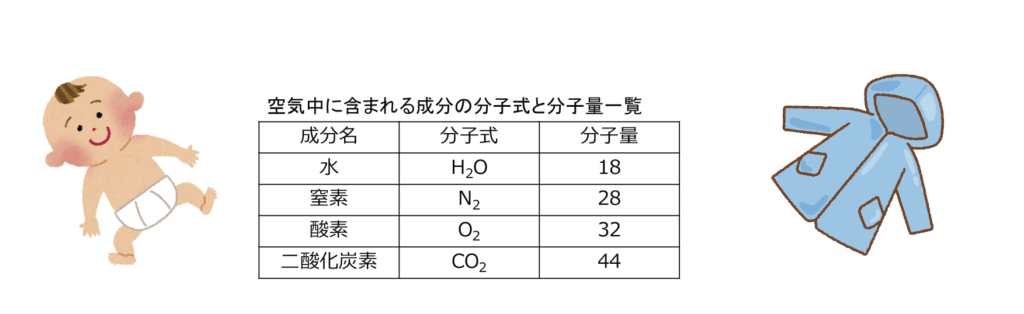
分子量は分子の重さを表すもので分子の大きさを示さないが、直感的に水は小さそうに見えます。それなのに、水は通らないのに他の成分は通るとはどういうこと?と思ったことがある人もいるのではないでしょうか。水分子が下のように描かれているのを見たことがあると思いますが、への字に曲がってることに意味があります。
この「への字」が不思議な性質の要因になっているため、今回は水の分子構造について説明します。
原子の最外殻はs軌道とp軌道で形成されています。s軌道は原子核を中心とした球状、p軌道はx,y,z方向に広がった形になってます。
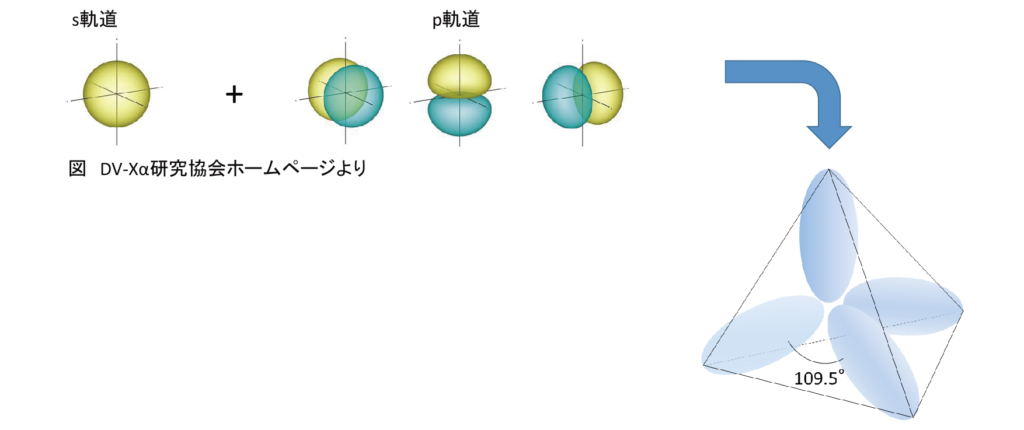
原子が他の原子と結びついて分子を形成するとき、この4つの軌道が混ざって等間隔に配置されます。形成される軌道は原子核を中心に正四面体の頂点方向へ伸びる形が基本です。1つのs軌道と3つのp軌道から成る意味で、sp3混成軌道と呼びます。
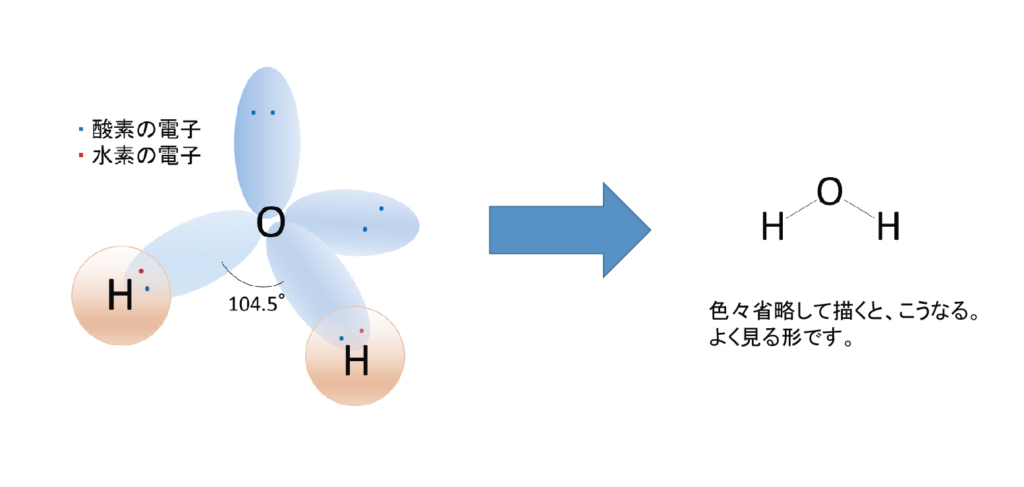
水素1Hの電子は1sに1個、酸素8Oでは電子配置が1S22S22P4のため最外殻の2sと2pに合計6個の電子が入っています。水素は閉殻までに電子が1個不足し、酸素は2個不足しています。そこで、酸素と2つの水素が電子を共有することで、それぞれの不足分を補うことができます。このとき形成される結合は電子を共有しているため、「共有結合」と呼ばれます。共有している電子対と共有していない電子対で状態が異なるため、O-H軌道間の角度は少し狭くなります。
原子は貴ガスの電子配置に近づこうとするため、短周期の左側は陽イオン、右側は陰イオンになりやすい。つまり、周期表の右に行くほど電子を引っ張る力が強くなるとも言えます。(貴ガスを除く)
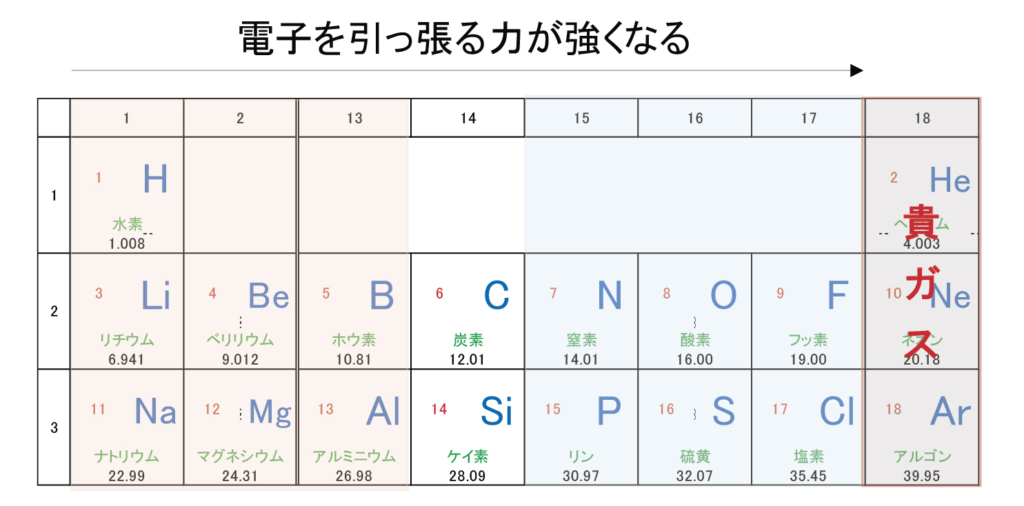
酸素が電子を引っ張っているため、水分子では電荷が微かに偏ることになります。
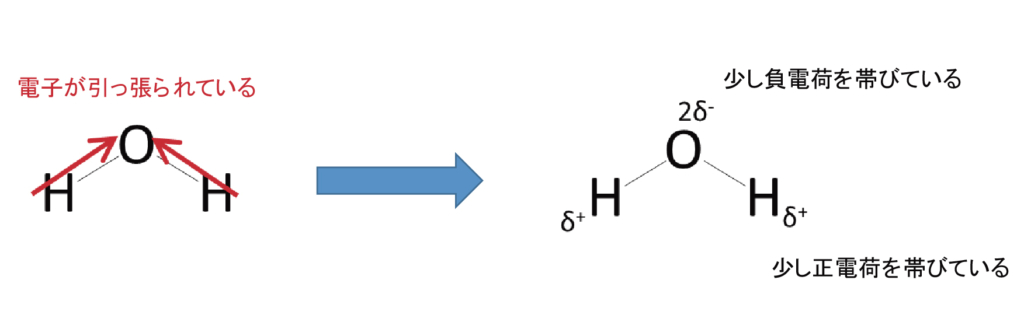
分子が曲がっていないと力が打ち消しあい、電荷は偏らなくなります。
水分子は電荷に偏りがあるため、水分子の水素は他の水分子の酸素と引き合います。そのため、水分子は集団を形成し、巨大な分子のように振る舞います。
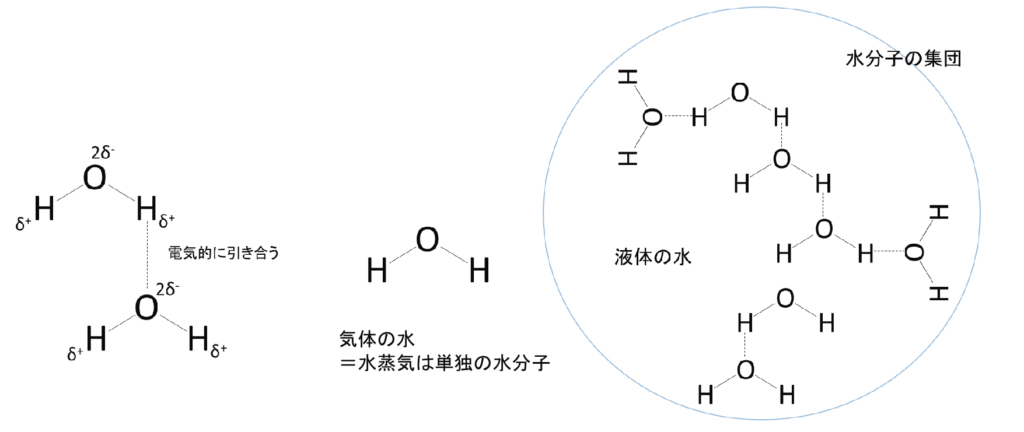
分子同士が引き合っているため、水は大きな表面張力を有します。撥水性のある膜に適切な穴を開けることにより、二酸化炭素など他の分子と篩分けることが出来ます。この性質を利用したのが「蒸れないけど漏れない素材」です。また、軽い水分子が大気圏外に揮散せず地球が水の星でいられるのも、水分子が集団を形成しているからです。水分子の結合が曲がっているため、我々は生きていけるのです。
周期表シリーズ
RANKING 人気事例ランキング
-
 1
1 -
 2
2 -
 3
3 -
 4
4 -
 5
5
TAG LIST