- ユニケミートップ
- Uni-Lab(分析技術情報)
- 周期表とは -原子核から見た周期表 –
周期表とは -原子核から見た周期表 –

メンデレーエフは元素の性質と原子量の関係を表にした。つまり、周期表は一部の矛盾を除き、原子量順に書かれているということになる。「原子量」とは何かについて考えてみる。
下に、水素とヘリウムの原子モデル注1を示す。
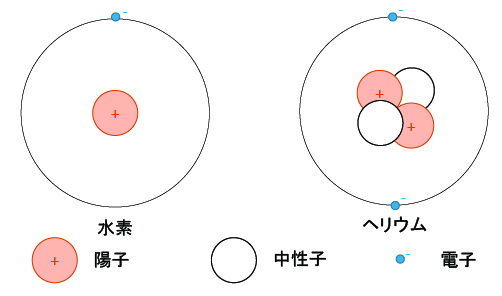
注1:陽子、中性子、電子は粒状の形態とは限らない。水素とヘリウムの電子殻直径は等しくない。
原子核の中には陽子と中性子があり、その周りを電子が周回している。陽子はプラスの電荷を、電子はマイナスの電荷を持っている。中性子は電荷を有していない。水素以外の原子核は、複数の陽子と中性子から成る。同じ電荷を有する陽子間には当然に斥力が働く。なぜ一所に集まっていられるのだろう?と思ったことは無いだろうか。
クーロンの法則(荷電粒子間に働く力)
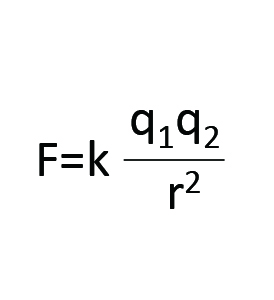
また、質量のある物質間には万有引力が働く
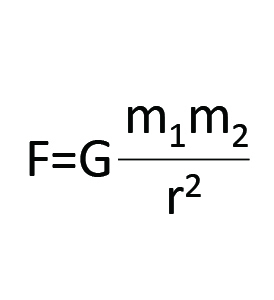
偶然にも、似た式になっている。注2
注2:あくまでイメージ。原子内部でニュートン力学が適応できるかは不明。原子核内には複数の力が発生していると言われている。
原子内部のため r≒0 と考えると、無限の斥力と無限の引力が発生することになる。そのため、原子核は非常に不安定と想像される。

中性子が存在することで引力が斥力に勝り、原子核は安定する。※注3
注3:実際は核子(陽子と中性子の総称)間の結合には量子力学的な解釈が必要だが、イメージしやすい引力を説明に用いた。厳密に言うと万有引力の法則は見つかっているが、引力の発生原理は解明されていない。

感覚的に、原子核の安定には中性子が必要不可欠な存在と理解できる。
核が安定するためには陽子1つに対して中性子は1つ以上必要なため、原子量は原子番号の2~2.6倍程度となっている。
最も原子核が安定する陽子と中性子の適切な比率と総数があり、同位体の中で半減期が著しく異なる元素もある。
陽子数が同じで中性子数が異なる元素を、「同位体」と呼ぶ。 例 : 水素には同位体が3つある。
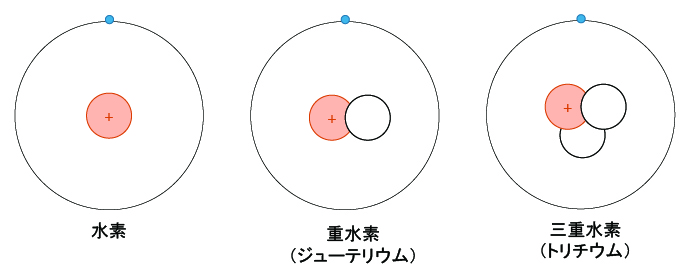
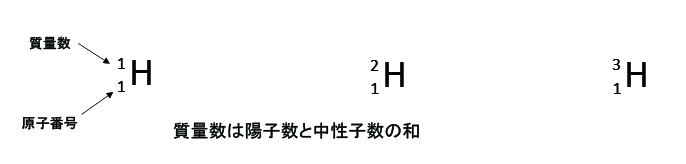
それぞれの同位体を記号で表記する場合は以下
少し脱線するが、水素イオンをH+と書きます。多くの人が水素原子から電子が抜けた状態を想像するだろうと思う。記号の通り描いてみると、水素イオンは陽子単体ということになる。
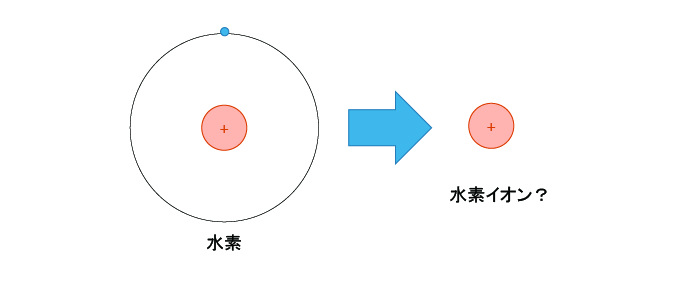
陽子単体って何か怖い。放射線であるα線(Heの原子核)より危険に見える。
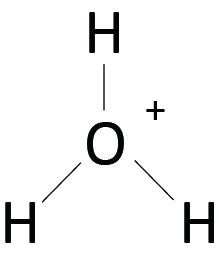
陽子単体は非常に反応性が高く、溶媒分子と結びつく。例えば、水中ではオキソニウムイオンH3O+の形で存在する。
アルファベット1文字または2文字で「元素記号」を示し、その横にある数字は「原子番号」を示す。
原子番号は陽子数を表し、原子量は同位体比率を加味した平均値に近似する。
原子量1は12C原子の質量を1/12とした相対質量と定義される。

<原子と元素> 原子(atom)は物質を細かく切断し、これ以上切断できない最小単位を示す。元素(element)という単語はその性質を顕現する根源の要素で、おそらく中国の五行思想や欧州の四大精霊などに由来する。原子は構造の違いを、元素は性質の違いを表す。同位体は異なる原子だが、元素としては同じとなる。
Cl(塩素)の原子番号は17で、質量数35と37の同位体がある。同位体比は約75:25となっている。下にクロロホルムのマススペクトルを示す。赤枠で囲んだフラグメントはCHCl2に由来する。
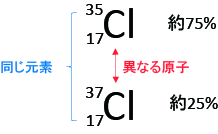
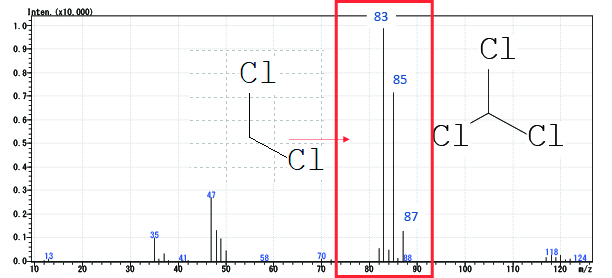
Clが二つとも質量数35の場合①とそれぞれ35と37の場合②と二つとも37の場合③がある。
炭素を12、水素を1とし計算すると
①12+1+35×2=83
②12+1+35+37=85
③12+1+37×2=87
となり、それらに対応するフラグメントが検出されている。GC/MSでも同位体の存在を確認することができる。
原子量と質量数は同義ではなく、中性子は陽子より微かに重くどちらの質量もピッタリ1ではない。ただし、原子量4桁程度であれば、質量数の平均値と概ね等しいと考えても差し支えない。
話し戻って、メンデレーエフは原子量順に並べたが、結果的に周期表は陽子数順に並んでいた。
陽子数の増加とともに中性子も増加するため、陽子数順と原子量順は概ね同じ並びになる。
メンデレーエフが矛盾を感じたテルルとヨウ素の順番も、陽子数順であれば矛盾はない。

<結論>
周期表は「原子の性質と原子量の関係」ではなく「原子の性質と陽子数の関係」を示していた。メンデレーエフは陽子の存在を予言したとも言える。
RANKING 人気事例ランキング
-
 1
1 -
 2
2 -
 3
3 -
 4
4 -
 5
5
TAG LIST